SO SÁNH CẤU TẠO VÀ TÍNH CHẤT CỦA ANKAN VÀ ANKEN
Trung tâm gia sư - dạy kèm tại nhà NTIC Đà Nẵng xin giới thiệu phần SO SÁNH CẤU TẠO VÀ TÍNH CHẤT CỦA ANKAN VÀ ANKEN. Nhằm hỗ trợ cho các bạn có thêm tư liệu học tập. Chúc các bạn học tốt môn học này.
Ngày đăng: 27-02-2018
39,384 lượt xem

I. CẤU TẠO VÀ ĐỒNG PHÂN
1. Khái niệm
a. Ankan
- Ankan (parafin) là những hiđrocacbon no, mạch hở trong phân tử chỉ có một loại liên kết đơn.
- Công thức chung: CnH2n+2 (n ≥ 1).
b. Anken
- Anken hay olefin là hiđrocacbon không no, mạch hở trong phân tử có chứa 1 liên kết đôi C=C còn lại là các liên kết đơn.
- Công thức tổng quát của anken: CnH2n (n ≥ 2).
2. Cấu tạo
a. Metan


b. Etilen

* Nhận xét:
- Cấu tạo ankan chỉ có một loại liên kết đơn.
- Cấu tạo anken có một liên kết đôi còn lại là liên kết đơn.
3. Đồng phân
a. Ankan
- Ankan chỉ có một loại đồng phân là đồng phân mạch cacbon.
Ví dụ: Từ C5H12 Viết các đồng phân ankan có thể có và gọi tên
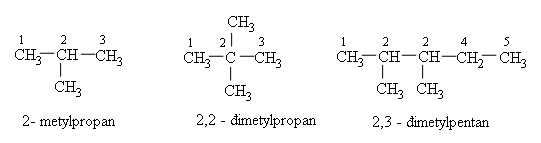
b. Anken
- Đồng phân cấu tạo: Bao gồm đồng phân vị trí liên kết đôi và đồng phân mạch C.
- Đồng phân hình học: Bao gồm đồng phân cis và trans
Ví dụ: Từ C4H8 Viết các đồng phân anken có thể có và gọi tên
CH2=CH-CH2-CH3 but-1-en
CH3-CH=CH-CH3 but-2-en
CH2=C(CH3)-CH3 2-metyl propen
Trong đó but-2-en có đồng phân hình học.

II. TÍNH CHẤT HÓA HỌC
* Nhận xét:
- Ankan tương đối trơ về mặt hóa học: Ở nhiệt độ thường chúng không phản ứng với axit, bazơ và chất oxi hóa mạnh (như ). Vì thế ankan còn có tên là parafin, nghĩa là ít ái lực hóa học.
- Anken có liên kết π kém bền → tính chất đặc trưng là tham gia phản ứng cộng, trùng hợp và oxi hóa.
1. Tính chất hóa học của ankan
a. Phản ứng thế
- Là phản ứng hóa học, trong đó một nguyên tố có độ hoạt động hóa học mạnh hơn (ở các điều kiện cụ thể về nhiệt độ, áp suất) sẽ thay thế cho nguyên tố có độ hoạt động hóa học yếu hơn trong hợp chất của nguyên tố này.
Ví dụ: CH4 + Cl2 → CH3Cl + HCl
b. Tác dụng của nhiệt
- Phản ứng tách H2 (phản ứng đề hiđro hóa)
CH3-CH2-CH3 → CH2=CH-CH3 + H2
Tổng quát
CnH2n+2 → CnH2n + H2 (Fe, t0)
- Phản ứng phân hủy
CH4 → C + 2H2 (t0)
- Phản ứng crăcking (n≥ 3)
C4H10 → CH4 + C3H6
→ C2H4 + C2H6
Tổng quát
CnH2n+2 → CxH2x+2 + CyH2y (t0, p, xt)
c. Phản ứng cháy
CnH2n+2 + (3n + 1)/2O2 → nCO2 + (n + 1)H2O
+ nCO2 < nH2O.
+ nH2O - nCO2 = nankan bị đốt cháy.
2. Tính chất hóa học của anken
a. Phản ứng cộng
- Cộng hợp H2: (điều kiện phản ứng Ni, t0) → ankan
CH2=CH2 + H2 → CH3-CH3
Tổng quát: CnH2n + H2 → CnH2n+2
- Cộng hợp halogen:
CH2=CH2 + Br2 → CH2Br-CH2Br
Tổng quát: CnH2n + Br2 → CnH2nBr2
- Cộng hợp hiđrohalogenua
CH2=CH2 + HCl → CH3-CH2Cl
Đồng đẳng của etilen
CH3-CH=CH2 + HCl → CH3-CH2-CH2-Cl
Sản phẩm phụ
→ CH3-CHCl-CH3
Sản phẩm chính
+ Nếu thực hiện phản ứng cộng HBr vào anken có xúc tác peoxit thì sản phẩm chính lại ngược quy tắc Maccopnhicop.
b. Phản ứng trùng hợp:
- Phản ứng trùng hợp: Là quá trình cộng hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành phân tử lớn (hợp chất cao phân tử).
nA → (B)n (t0, xt, p)
Ví dụ:
nCH2=CH2 → (-CH2–CH2-)n (Polietylen hay PE)
nCH2=CH–CH3 → (-CH2–CH(CH3)-)n (Polipropilen hay PP)
c. Phản ứng oxi hóa
- Phản ứng oxi hóa không hoàn toàn:
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2KOH + 2MnO2
- Phản ứng cháy:
CnH2n + 3n/2O2 → nCO2 + nH2O
+ Đặc điểm phản ứng đốt cháy anken: nCO2 = nH2O.
Trung tâm luyện thi, gia sư - dạy kèm tại nhà NTIC Đà Nẵng
LIÊN HỆ NGAY VỚI CHÚNG TÔI ĐỂ BIẾT THÊM THÔNG TIN CHI TIẾT
ĐÀO TẠO NTIC
Địa chỉ: Đường nguyễn lương bằng, P.Hoà Khánh Bắc, Q.Liêu Chiểu, Tp.Đà Nẵng
Hotline: 0905540067 - 0778494857
Email: daotaontic@gmail.com
Tin liên quan
- › KHÁI NIỆM, ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP VÀ TINH CHẤT VẬT LÍ CỦA ANDEHIT
- › CẤU TẠO, TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ỨNG DỤNG CỦA ANDEHIT
- › SO SÁNH CẤU TẠO VÀ TÍNH CHẤT CỦA ANKOL VÀ PHENOL
- › KHÁI NIỆM, PHÂN LOẠI, TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ỨNG DỤNG CỦA PHENOL
- › SO SÁNH CẤU TẠO VÀ TÍNH CHẤT CỦA ANKEN VÀ ANKIN
- › TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ỨNG DỤNG CỦA ANCOL
- › KHÁI NIỆM, ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP VÀ TINH CHẤT VẬT LÍ CỦA ANCOL
- › CẤU TẠO, TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ỨNG DỤNG CỦA STIREN
- › TÍNH CHẤT HÓA HỌC, ĐIỀU CHẾ VÀ ỨNG DỤNG CỦA ANKIN
- › KHÁI NIỆM, ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP VÀ TÍNH CHẤT VẬT LÍ CỦA ANKIN









Gửi bình luận của bạn