CẤU TẠO, TÍNH CHẤT VÀ ỨNG DỤNG CỦA AMIN
Trung tâm gia sư - dạy kèm tại nhà NTIC Đà Nẵng giới thiệu KHÁI NIỆM, CẤU TẠO TÍNH CHẤT VÀ ỨNG DỤNG CỦA AMIN nhằm hỗ trợ cho các bạn có thêm tư liệu học tập. Chúc các bạn học tốt môn học này.
Ngày đăng: 13-08-2017
14,150 lượt xem

Phần 1: Lý thuyết
I – KHÁI NIỆM, PHÂN LOẠI, DANH PHÁP VÀ ĐỒNG PHÂN
1. Khái niệm
- Amin là hợp chất hữu cơ được tạo ra khi thế một hoặc nhiều nguyên tử hiđro trong phân tử amoniac bằng một hoặc nhiều gốc hiđrocacbon.
Ví dụ:
2. Phân loại Amin được phân loại theo hai cách thông dụng nhất
a) Theo đặc điểm cấu tạo của gốc hiđrocacbon
- Amin thơm
- Amin béo
- Amin dị vòng
Ví dụ:
b) Theo bậc của amin
- Bậc amin: là số nguyên tử H trong phân tử NH3 bị thay thế bởi gốc hiđrocacbon. Theo đó, các amin được phân loại thành: amin bậc 1, bậc 2, bậc 3.
Ví dụ:
3. Danh pháp
a) Cách gọi tên theo danh pháp gốc – chức :
ank + yl + amin
b) Cách gọi tên theo danh pháp thay thế :
ankan + vị trí + amin
c) Tên thông thường chỉ áp dụng với một số amin
Hợp chất Tên gốc – chức Tên thay thế Tên thường
CH3–NH2 metylamin metanamin
CH3–CH(NH2)–CH3 isopropylamin propan-2-amin
CH3–NH–C2H5 etylmetylamin N-metyletanamin
CH3–CH(CH3)–CH2–NH2 isobutylamin 2-metylpropan-1-amin
CH3–CH2–CH(NH2)–CH3 sec-butylamin butan-2-amin
(CH3)3C–NH2 tert-butylamin 2-metylpropan-2-amin
CH3–NH–CH2–CH2–CH3 metylpropylamin N-metylpropan-1-amin
CH3–NH–CH(CH3)2 isopropylmetylamin N-metylpropan-2-amin
C2H5–NH–C2H5 đietylamin N-etyletanamin
(CH3)2N–C2H5 etylđimetylamin N,N-đimetyletanamin
C6H5–NH2 phenylamin benzenamin anilin
Chú ý:
- Tên các nhóm ankyl đọc theo thứ tự chữ cái a, b, c…
- Với các amin bậc 2 và 3, chọn mạch dài nhất chứa N làm mạch chính, N có chỉ số vị trí nhỏ nhất. Đặt một nguyên tử N trước mỗi nhóm thế của amin - Khi nhóm –NH2 đóng vai trò nhóm thế thì gọi là nhóm amino.
Ví dụ: CH3CH(NH2)COOH (axit 2-aminopropanoic)
4. Đồng phân Amin có các loại đồng phân:
- Đồng phân về mạch cacbon
- Đồng phân vị trí nhóm chức
- Đồng phân về bậc của amin
II – TÍNH CHẤT VẬT LÍ
- Các amin có khả năng tan tốt trong nước, do giữa amin và nước có liên kết Hiđro liên phân tử. Độ tan trong nước giảm khi số nguyên tử C tăng.
- Metyl–, đimetyl–, trimetyl– và etylaminlà những chất khí có mùi khai khó chịu, độc, dễ tan trong nước, các amin đồng đẳng cao hơn là chất lỏng hoặc rắn
- Anilin là chất lỏng, nhiệt độ sôi là 184oC, không màu, rất độc, ít tan trong nước, tan trong ancol và benzen
III – CẤU TẠO PHÂN TỬ VÀ SO SÁNH LỰC BAZƠ
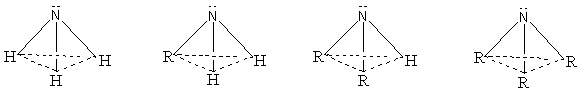
1. Cấu trúc phân tử của amoniac và các amin
2. Cấu tạo phân tử của amoniac và các amin
Trên nguyên tử nitơ đều có cặp electron tự do nên amoniac và các amin đều dễ dàng nhận proton. Vì vậy amoniac và các amin đều có tính bazơ.
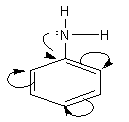
3. Đặc điểm cấu tạo của phân tử anilin
- Do gốc phenyl (C6H5–) hút cặp electron tự do của nitơ về phía mình, sự chuyển dịch electron theo hiệu ứng liên hợp p – p (chiều như mũi tên cong) làm cho mật độ electron trên nguyên tử nitơ giảm đi, khả năng nhận proton giảm đi. Kết quả là làm cho tính bazơ của anilin rất yếu (không làm xanh được quỳ tím, không làm hồng được phenolphtalein).
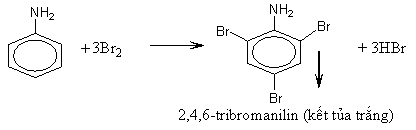
- Nhóm amino (NH2) làm tăng khả năng thế Br vào gốc phenyl (do ảnh hưởng của hiệu ứng +C). Phản ứng thế xảy ra ở các vị trí ortho và para do nhóm NH2 đẩy electron vào làm mật độ electron ở các vị trí này tăng lên
4. So sánh lực bazơ
a) Các yếu tố ảnh hưởng đến lực bazơ của amin:
- Mật độ electron trên nguyên tử N: mật độ càng cao, lực bazơ càng mạnh và ngược lại
- Hiệu ứng không gian: gốc R càng cồng kềnh và càng nhiều gốc R thì làm cho tính bazơ giảm đi, phụ thuộc vào gốc hiđrocacbon. Ví dụ tính bazơ của (CH3)2NH > CH3NH2 > (CH3)3N ; (C2H5)2NH > (C2H5)3N > C2H5NH2
b) Phương pháp
- Gốc đẩy electron làm tăng tính bazơ, gốc hút electron làm giảm tính bazơ.
Ví dụ: p-NO2-C6H4NH2 < C6H5NH2< NH3 < CH3NH2 < C2H5NH2 < C3H7NH2
- Amin có càng nhiều gốc đẩy e thì tính bazơ càng mạnh, amin có càng nhiều gốc hút e thì tính bazơ càng yếu.
(Rthơm)3N < (R thơm)2NH < RthơmNH2 < NH3 < Rno NH2 < (Rno)2NH < (Rno)3N
Chú ý:
- Gốc Rno càng cồng kềnh thì ảnh hưởng không gian của nó càng lớn làm cản trở quá trình H+ tiến lại gần nguyên tử N nên (Rno)2NH < (Rno)3N sẽ không còn đúng nữa.
IV – TÍNH CHẤT HÓA HỌC
1. Tính chất của chức amin
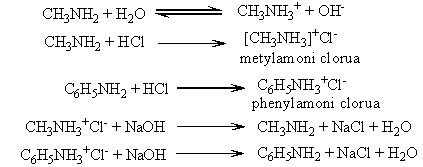
a) Tính bazơ: tác dụng lên giấy quỳ tím ẩm hoặc phenolphtalein và tác dụng với axit
- Dung dịch metylamin và nhiều đồng đẳng của nó có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein do kết hợp với proton mạnh hơn amoniac
- Anilin và các amin thơm rất ít tan trong nước. Dung dịch của chúng không làm đổi màu quỳ tím và phenolphtalein
b) Phản ứng với axit nitrơ:
- Amin no bậc 1 + HNO2 → ROH + N2 + H2O. Ví dụ: C2H5NH2 + HONO → C2H5OH + N2 + H2O
- Amin thơm bậc 1 tác dụng với HNO2 ở nhiệt độ thấp tạo thành muối điazoni.
Ví dụ: C6H5NH2 + HONO + HCl ![]() C6H5N2+ Cl- + 2H2O
C6H5N2+ Cl- + 2H2O
benzenđiazoni clorua
c) Phản ứng ankyl hóa: amin bậc 1 hoặc bậc 2 tác dụng với ankyl halogenua (CH3I, ….)
Phản ứng này dùng để điều chế amin bậc cao từ amin bậc thấp hơn.
Ví dụ: C2H5NH2 + CH3I → C2H5NHCH3 + HI
d) Phản ứng của amin tan trong nước với dung dịch muối của các kim loại có hiđroxit kết tủa
3CH3NH2 + FeCl3 + 3H2O → Fe(OH)3 + 3CH3NH3Cl
2. Phản ứng thế ở nhân thơm của anilin
Phần 2: Bài tập vận dụng
LIÊN HỆ NGAY VỚI CHÚNG TÔI ĐỂ BIẾT THÊM THÔNG TIN CHI TIẾT
ĐÀO TẠO NTIC
Địa chỉ: Đường nguyễn lương bằng, P.Hoà Khánh Bắc, Q.Liêu Chiểu, Tp.Đà Nẵng
Hotline: 0905540067 - 0778494857
Email: daotaontic@gmail.com
Tin liên quan
- › TÍNH CHẤT HÓA HỌC CHUNG CỦA KIM LOẠI
- › CẤU TẠO VÀ TÍNH CHẤT VẬT LÍ CỦA KIM LOẠI
- › VỊ TRÍ KIM LOẠI TRONG BTTH, CẤU TẠO VÀ LIÊN KẾT KIM LOẠI
- › KHÁI NIỆM VỀ POLIME VÀ VẬT LIỆU POLIME
- › CẤU TẠO, TÍNH CHẤT VÀ ỨNG DỤNG CỦA AMINO AXIT
- › CẤU TẠO, TÍNH CHẤT, ỨNG DỤNG CỦA TINH BỘT VÀ XENLULOZO
- › CẤU TAO, TÍNH CHẤT VÀ ỨNG DỤNG CỦA SACCAROZO
- › CẤU TẠO, TÍNH CHẤT VÀ ỨNG DỤNG CỦA GLUCOZO
- › KHÁI NIỆM, CẤU TẠO, TÍNH CHẤT VÀ ỨNG DỤNG CỦA LIPIT
- › KHÁI NIỆM, CẤU TẠO TÍNH CHẤT VÀ ỨNG DỤNG CỦA ESTE
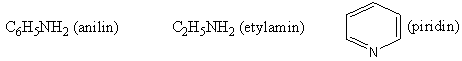
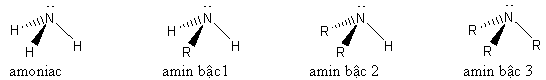









Gửi bình luận của bạn